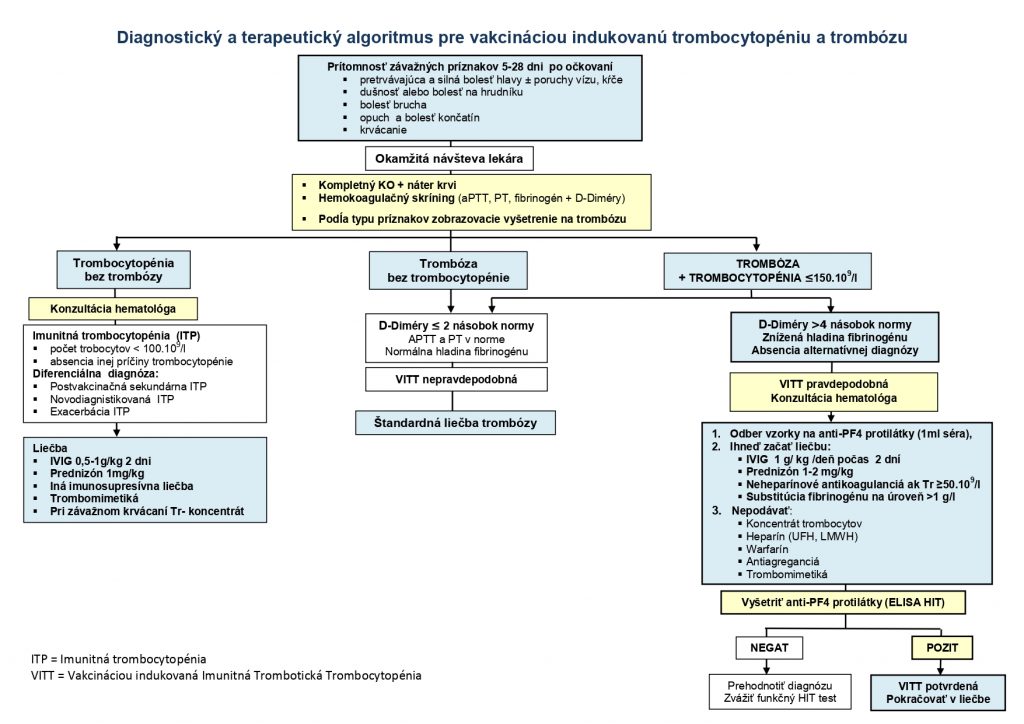
Odporúčania Slovenskej hematologickej a transfúziologickej spoločnosti SLS pre diagnostiku a manažment vakcínou indukovanej imunitnej trombotickej trombocytopénie (VITT) po očkovaní proti COVID-19.
27. apríl 2021
Úvod
Doterajší vývoj a aj aktuálna situácia pandémie vírusovej infekcie COVID-19 spôsobenej vírusom SARS-CoV-2 na Slovensku, v Európe ale i v celosvetovom meradle potvrdzujú, že jedinou množnou cestou účinnej eradikácie vírusu je vakcinácia obyvateľstva.
V EÚ sa používajú dva typy vakcín na vpravenie informácie pre syntézu dôležitého antigénu vírusu SARS-CoV-2 -„S-proteínu“, ktorý vyvolá efektívnu imunizáciu:
- mRNA vakcíny a
- tzv.vektorové vakcíny, ktoré využívajú vírusový obal (adenovírus) na transfer DNA pre syntézu S-proteínu.
Po podaní vakcíny AstraZeneca (AZ) sa veľmi zriedkavo vyskytli atypické trombózy sprevádzané trombocytopéniou. V súčasnosti nie je známy žiaden rizikový faktor alebo predisponujúci stav pre vývoj tejto komplikácie.
Praktickí lekári a iní zdravotnícki pracovníci musia byť informovaní o tejto vzácnej, ale závažnej komplikácii a v prípade podozrenia musia zabezpečiť odoslanie pacienta do najbližšieho zdravotníckeho zariadenia a konzultáciu hematológa.
Tento dokument slúži ako všeobecné usmernenie pre včasné rozpoznanie, diagnostiku, manažment a hlásenie vakcináciou indukovanej imunitnej trombotickej trombocytopénie (VITT).
Usmernenie je v súlade s aktualizovanými medzinárodnými odporučeniami (12-14).
Keďže v prípade VITT ide o novú a vyvíjajúcu sa oblasť hemostázy a trombózy, je potrebné sledovať dostupnosť ďalších aktualizácií odporučení.
Trombocytopénia a trombóza ako vedľajšie účinky vakcinácie proti COVID-19
Vakcína AZ je vektorová vakcína, využívajúca vírusový obal (adenovírus) na vpravenie DNA pre syntézu S-proteínu, proti ktorému organizmus začne tvoriť protilátky. Používa sa v krajinách EÚ, Veľkej Británii v Kanade aj Indii.
V polovici marca 2021 sa objavili prvé správy o zriedkavom výskyte atypickej trombózy spojenej s trombocytopéniou po očkovaní AZ.
Do 4. 4. 2021 bolo po podaní viac ako 34 mil. injekcií tejto vakcíny hlásených 169 prípadov trombózy mozgových žilových sínusov (Central Venous Sinus Thrombosis-CVST) a 52 prípadov trombózy splanchnických žíl (Splanchnic Vein Thrombosis- SVT).
Pomerom rizika 6,2 /1 milión injekcií a incidenciou v európskych krajinách 1:210 000 injekcií, predstavuje trombóza extrémne zriedkavú komplikáciu, ktorá sa odhalila až pri post-registračnom použití vakcíny AZ (1-3).
Výskyt treba posudzovať aj v kontexte s odhadovanou icidenciou CSVT v bežnej populácii bez vakcinácie, ktorá je 0,22-1,57:100 000 (4).
Do 9.4.2021 najmenej 5 krajín stanovilo limity pre vakcináciu AZ, väčšinou na základe veku.
6 možných prípadov trombózy mozgových splavov (s trombózou splanchnických žíl alebo bez nej) sa pozorovalo medzi 6,8 miliónmi jedincov očkovaných vektorovou vakcínou Johnson & Johnson (J&J).
Po prechodnom pozastavení a dôkladnej analýze rizika a benefitu vakcíny J&J FDA očkovanie opätovne povolila (5).
Medzi 54 mil. recipientmi mRNA vakcíny Pfizer-BioNtech bolo referovaných 35 prípadov CNS trombózy a 5 možných, ale neoverených prípadov sa vyskytlo u 4 mil. očkovaných mRNA vakcínou Moderna (5).
Po očkovaní mRNA vakcínou Pfizer-BioNtech a Moderna bolo opísaných aj 20 prípadov sekundárnej imunitnej trombocytopénie bez trombózy (4,6).
Európske regulačné orgány ako EMA a PRAC (Pharmacovigilance Risk Assessment Committee) ako aj medzinárodná spoločnosť pre hemostázu a trombózu (ISTH) vydali stanovisko, podľa ktorého vzhľadom na extrémne zriedkavý výskyt týchto komplikácií výhody očkovania COVID-19 vo všetkých vekových skupinách prevyšujú potenciálne riziko nežiaducich účinkov (7-10).
EMA a PRAC odporúčajú v očkovaní pokračovať ktoroukoľvek dostupnou, EMA registrovanou vakcínou.
Vakcínou indukovaná imunitná trombotická trombocytopénia (VITT).
Tento syndróm vznikol 5-28 dní po očkovaní AZ u predtým zdravých alebo klinicky stabilných jedincov, väčšinou žien vo veku do 55 rokov (1-3).
Je charakterizovaný venóznou trombózou v atypickej lokalizácii (prevažne CVST a SVT), pľúcnou embóliou alebo arteriálnou trombózou, sprevádzanou trombocytopéniou.
Počet trombocytov v čase diagnózy je 20-30.109/l (rozptyl 10-110. 109/l).
Súčasne je zvýšená hladina D-dimérov nad 4-násobok normy, teda oveľa viac ako býva pri akútnej žilovej trombóze, a hladina fibrinogénu je znížená.
Patogenéza VITT nie je zatiaľ objasnená, ale syndróm pripomína „heparínom indukovanú trombocytopéniu“ (HIT). U všetkých pacientov sa zisťuje pozitivita protilátok proti komplexu doštičkový faktor 4 (PF4) – polyanión, ktoré podobne ako pri HIT spôsobujú masívnu aktiváciu krvných doštičiek, trombózu a následnú konzumpciu trombocytov s trombocytopéniou.
Pri VITT prítomnosť anti-PF4 protilátok dokázaných testom ELISA pripomína nález pri „atypickej“ alebo „autoimunitnej“ HIT, pri ktorej vznikajú tromby aj bez predchádzajúcej expozície heparínu (11).
Rovnako ako syndróm HIT aj VITT predstavuje mimoriadne závažný stav s potenciálne fatálnym priebehom a mortalitou až 30-40%.
Trombózy sa môžu vyskytnúť vo viacerých lokalitách a môže vzniknúť krvácanie do CNS alebo iných orgánov v dôsledku ischémie, trombocytopénie prípadne antikoagulačnej liečby (1-3).
Existuje vyššia pravdepodobnosť vzniku VITT vo vybraných skupinách?
- VITT je veľmi zriedkavý syndróm. V súčasnosti nie je známa žiadna predispozícia ani pravdepodobnosť pre vznik VITT (1-3,12-15).
- Nepredpokladá sa, že by sa VITT vyskytoval častejšie u ľudí s osobnou alebo rodinnou anamnézou trombózy, u pacientov na antikoagulačnej liečbe alebo u tehotných žien a pri užívaní antikoncepcie, nakoľko VITT vzniká iným patogenetickým mechanizmom ako bežné typy trombózy pri vrodených alebo získaných trombofilných stavoch.
- Vzhľadom na túto skutočnosť nie je toho času možné definovať žiadne skupiny jedincov s vyšším rizikom pre vznik VITT, alebo osoby, ktoré by sa mali vyhýbať očkovaniu vakcínou AstraZeneca.
- Pred očkovaním nie je indikované testovanie na vrodenú trombofíliu.
- Preventívne užívanie protidoštičkových liekov alebo LMWH po očkovaní nie je indikované, lebo nezabráni raritnému vzniku trombocyty aktivujúcich protilátok.
Klinické podozrenie a prezentácia VITT
1. Vznik závažných príznakov 4-28 dní po vakcinácii
2. Prítomnosť príznakov podozrivých z prítomnosti atypickej trombózy
- pretrvávajúca a silná bolesť hlavy ± neurologické príznaky: rozmazané / dvojité videnie a kŕče
- dušnosť alebo bolesť na hrudníku (pľúcna embólia alebo akútny koronárny syndróm)
- bolesť brucha (trombóza splanchnickej oblasti)
- opuch a bolesti končatín (hlboká žilová trombóza, akútna ischémia končatín).
Zdravotnícki pracovníci musia upozorniť občanov podrobujúcich sa vakcinácii, že ak sa u nich objavia vyššie uvedené príznaky, musia okamžite vyhľadať lekársku pomoc.
Čo robiť, keď má pacient vyššie uvedené príznaky?
- Overiť dátum vakcinácie a potvrdiť začiatok ťažkostí v intervale 5-28 dní po očkovaní.
- Vyšetriť kompletný KO. Podozrenie na VITT je pri počte trombocytov ≤150.109/l.
- Pri podozrení na VITT ďalej vyšetriť:
- Fibrinogén (znížená hladina)
- D-dimér – typická je vysoká koncentrácia (> 4 x horná hranica normy)
- Protilátky anti-PF4 (v teste ELISA HIT)
- CT alebo MRI vyšetrenie na vylúčenie CSVT alebo iného typu trombózy.
4. Podľa typu ťažkostí zvoliť zobrazovacie vyšetrenie na dôkaz trombózy
5. Dostupné testy na dôkaz HIT protilátok nie sú na VITT citlivé. Vzhľadom na raritnosť syndrómu sa test ELISA bude robiť centralizovane v laboratóriách MEDIREX v Bratislave, Košiciach a v Nitre. Odber vzorky sa vykoná pred začatím liečby a zaistí sa transport vzorky (sérum 1 ml).

Hlásenie VITT
Prípady trombocytopénie a novo vzniknutej trombózy spojenej s trombocytopéniou po očkovaní ktoroukoľvek vakcínou sa okamžite hlásia do Štátneho ústavu pre kontrolu liekov (ŠÚKL).
Môžu pacienti, ktorí prekonali VITT dostať druhú dávku vakcíny AstraZeneca?
- CHMP v zhode s SPC odporúča pokračovať druhou dávkou vakcíny AZ (Vaxzevria) 4-12 týždňov po prvej vakcíne (16).
- Toho času nie je dostatok pozorovaní a dôkazov pre zmenu súčasných odporučení, napr. podanie vakcíny AZ v dlhšom intervale ako 4-12 týždňov alebo podanie mRNA vakcíny v druhej dávke očkovania.
Tieto odporúčania sú zamerané na včasné rozpoznani, diagnostiku a liečbu VITT a umožnia znížiť výskyt fatálnych prípadov a zlepšiť prognózu tejto zriedkavej, ale vážnej komplikácie očkovania proti infekcii COVID-19.
Potrebné je naďalej sledovať pribúdajúce nové poznatky o patogenéze a manažmente VITT, na základe ktorých sa tieto odporučenia budú aktualizovať.
Literatúra
1. Schultz NH, et al. Thrombosis and thrombocytopenia after ChAdOx1 nCoV-19 vaccination. N Engl J Med April 9, 2021. doi:10.1056/NEJMoa2104882.
2. Greinacher A et al. Thrombotic thrombocytopenia after ChAdOx1 nCov-19 vaccination. N Engl J Med April 9, 2021. doi:10.1056/NEJMoa2104840.
3. Scully M, Singh D, Lown R, et al. Pathologic Antibodies to Platelet Factor 4 after ChAdOx1 nCoV-19 Vaccination. N Engl J Med April 16, 2021; DOI: 10.1056/ NEJMoa2105385.
4. Cines DB & Bussel JB. SARS-CoV-2 Vaccine–Induced Immune Thrombotic Thrombocytopenia. N Engl J Med April 16, 2021; DOI: 10.1056/NEJMe2106315.
5. FDA and CDC Lift Recommended Pause on Johnson & Johnson (Janssen) COVID-19 Vaccine Use Following Thorough Safety Review. https://www.cdc.gov/media/releases/2021/fda-cdc-lift-vaccine-use.html. 6. Lee EJ, Cines DB, Gernsheimer T, et al. Thrombocytopenia following Pfizer and Moderna SARS-CoV-2 vaccination. Am J Hematol 2021;96:534-537
7. https://www.ema.europa.eu/en/news/covid-19-vaccine-astrazeneca-prac-investigating-cases-thromboembolic-events-vaccines-benefits
8. Press briefing on the conclusion of the assessment of the Pharmacovigilance Risk Assessment Committee (PRAC) of Vaxzevria (previously COVID-19 Vaccine AstraZeneca) and thromboembolic events (07/04/2021)
9. AstraZeneca’s COVID-19 vaccine: EMA finds possible link to very rare cases of unusual blood
clots with low blood platelets (EMA, April 7, 2021) https://www.ema.europa.eu/en/news/ astrazenecas-covid-19-vaccine-ema-finds-possible-link-very-rare-casesunusual-blood-clots-low-blood
10. Statement from the ISTH on Reports Indicating Blood Clots Associated With the AstraZeneca Vaccine (ISTH, April 9, 2021). https://www.isth.org/news/559981/
11. Greinacher A, Selleng K, Warkentin TE. Autoimmune heparin-induced thrombocytopenia. J Thromb Haemost 2017;15:2099-2114.
12. Guidance produced by the Expert Haematology Panel (EHP) focused on Vaccine induced Thrombosis and Thrombocytopenia (VITT) (last updated 10/04/2021) https://b-s-h.org.uk/about-us/news/covid-19-updates/
13. Guidance Produced from the Expert Haematology Panel (EHP) focused on Syndrome of Thrombosis and Thrombocytopenia Occurring after Coronavirus Vaccination https://assets.publishing.service.gov.uk/government/uploads/system/uploads/attachment data/file/978194/uk-HCP-covid-19-vaccine-astrazeneca-reg174_proposed_14_Apr_2021
14. ISTH Interim Guidance for the Diagnosis and Treatment on Vaccine Induced Immune Thrombotic Thrombocytopenia (Updated 20 April, 2021) https://cdn.ymaws.com/www.isth.org/resource/resmgr/ISTH_VITT_Guidance_2.pdf.
15. Nazy I, Sachs UJ, rnold DM et al. Recommendations fot he clinical and laboratory diagnosis of vaccine-induced immune throbotic thromboytopenia (VITT) for SARS-CoV-2 infections: Commuication from the ISTH SSC Subcommittee on Platelet Immunology. T Trom Haemost April 24,2021;doi: 10.1111/JTH.15341.
16. EMA: AstraZeneca’s COVID-19 vaccine: benefits and risks in context. 26 April 2021. https://www.ema.europa.eu/en/news/astrazenecas-covid-19-vaccine-benefits-risks-context
Vypracovala: prof. MUDr. Angelika Bátorová, PhD., Hlavná odborníčka MZ-SR pre hematológiu
Odporúčania boli odsúhlasené výborom Slovenskej hematologickej a transfúziologickej spoločnosti SLS 26.4.2021.
MUDr. A.Wild
prezident SHaTS SLS